<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Topics to be covered </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> 1. Elimination reactions 2. $S_N i$ reaction 3. Elimination reaction 4. $E_1$ elimination 5. $E_1$ mechanism Example 6. $E_2$ Elimination 7. Example of $E_2$ elimination 8. Saytzeff vs Hofmann 9. $E_1$cb elimination 10. Substitution vs Elimination reactiuon 11. Reaction with metals </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> 1. उन्मूलन प्रतिक्रियाएँ 2. $S_N i$ प्रतिक्रिया 3. उन्मूलन प्रतिक्रिया 4. $E_1$ उन्मूलन 5. $E_1$ तंत्र उदाहरण 6. $E_2$ उन्मूलन 7. $E_2$ उन्मूलन का उदाहरण 8. सैटज़ेफ़ बनाम हॉफमैन 9. $E_1$cb उन्मूलन 10. प्रतिस्थापन बनाम उन्मूलन प्रतिक्रिया 11. धातुओं के साथ अभिक्रिया </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example</footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Elimination reactions </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - When a haloalkane with $\beta$-hydrogen atom is heated with alcoholic solution of potassium hydroxide, there is elimination of hydrogen atom from $\beta$-carbon and a halogen atom from the $\alpha$-carbon atom. - As a result, an alkene is formed as a product. Since $\beta$-hydrogen atom is involved in elimination, it is often called $\beta$-elimination. - If there is possibility of formation of more than one alkene due to the availability of more than one $\beta$-hydrogen atoms, usually one alkene is formed as the major product. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - जब $\beta$-हाइड्रोजन परमाणु वाले हैलोऐल्केन को पोटेशियम हाइड्रॉक्साइड के अल्कोहलिक घोल के साथ गर्म किया जाता है, तो $\beta$-कार्बन से हाइड्रोजन परमाणु और $\alpha$-कार्बन परमाणु से एक हैलोजन परमाणु निकल जाता है। - परिणामस्वरूप, एक उत्पाद के रूप में एक एल्कीन बनता है। चूँकि $\beta$-हाइड्रोजन परमाणु उन्मूलन में शामिल होता है, इसलिए इसे अक्सर $\beta$-उन्मूलन कहा जाता है। - यदि एक से अधिक $\beta$-हाइड्रोजन परमाणुओं की उपलब्धता के कारण एक से अधिक एल्कीन बनने की संभावना हो, तो आमतौर पर एक एल्कीन प्रमुख उत्पाद के रूप में बनता है। </div> </main> <hr> <footer style="font-size:18px"> <span style="color:blue">Elimination reactions</span> $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Elimination reactions </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - These form part of a pattern first observed by Russian chemist, Alexander Zaitsev (also pronounced as Saytzeff) who in 1875 formulated a rule which can be summarised as "in dehydrohalogenation reactions, the preferred product is that alkene which has the greater number of alkyl groups attached to the doubly bonded carbon atoms." - Thus, 2-bromopentane gives pent-2-ene as the major product. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - ये एक पैटर्न का हिस्सा हैं जिसे सबसे पहले रूसी रसायनज्ञ, अलेक्जेंडर ज़ैतसेव (जिसे सैत्ज़ेफ़ भी कहा जाता है) ने देखा था, जिन्होंने 1875 में एक नियम तैयार किया था जिसे संक्षेप में कहा जा सकता है "डीहाइड्रोहैलोजनेशन प्रतिक्रियाओं में, पसंदीदा उत्पाद वह एल्केन है जिसमें एल्काइल की संख्या अधिक होती है दोहरे बंधित कार्बन परमाणुओं से जुड़े समूह।" - इस प्रकार, 2-ब्रोमोपेंटेन प्रमुख उत्पाद के रूप में पेंट-2-ईन देता है। </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/0e5550ed-a808-49f0-805f-2b92b106e100/public" style='width:50%;'> </div> </main> <hr> <footer style="font-size:18px"> <span style="color:blue">Elimination reactions</span> $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $S_N$i reaction </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - Aliphatic Nucleophilic substitution reaction leading to retention of configuration (Internal Nucleophilic substations). - The displacement of - $\mathrm{OH}$ by $\mathrm{Cl}$ - using thionyl chloride. - This substitution proceeds through $S_N i$ Mechanism, in which there is retention of configuration. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - एलिफैटिक न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रिया से विन्यास (आंतरिक न्यूक्लियोफिलिक सबस्टेशन) का प्रतिधारण होता है। - थियोनिल क्लोराइड का उपयोग करके - $\mathrm{OH}$ को $\mathrm{Cl}$ द्वारा विस्थापित करना। - यह प्रतिस्थापन $S_N i$ तंत्र के माध्यम से आगे बढ़ता है, जिसमें कॉन्फ़िगरेशन का प्रतिधारण होता है। </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/0d4323dc-dc49-4c7f-2114-3fd2ed365700/public" style='width:50%;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ <span style="color:blue">$S_N i$ reaction</span> $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Elimination reaction </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> When a haloalkane with b-hydrogen atom is heated with alcoholic solution of potassium hydroxide, there is elimination of hydrogen atom from b-carbon and a halogen atom from the a-carbon atom. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> जब बी-हाइड्रोजन परमाणु वाले हैलोऐल्केन को पोटेशियम हाइड्रॉक्साइड के अल्कोहलिक घोल के साथ गर्म किया जाता है, तो बी-कार्बन से हाइड्रोजन परमाणु और ए-कार्बन परमाणु से हैलोजन परमाणु निकल जाता है। </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/bed8696e-563c-4009-2e4b-b63316996e00/public" style='width:50%;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ <span style="color:blue">Elimination reaction</span> $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Elimination reaction </B></Primary> <hr> <main> <div style='float: left; width:35%; text-align: left;font-size:23px'> There are three type of Elimination reaction: - $\scriptsize{E_1}$ Elimination - $\scriptsize{E_2}$ Elimination - $\scriptsize{E_1cb}$ elimination </div> <div style='float: right; width:35%; text-align: left;font-size:23px'> उन्मूलन प्रतिक्रिया तीन प्रकार की होती है: - $\scriptsize{E_1}$ उन्मूलन - $\scriptsize{E_2}$ उन्मूलन - $\scriptsize{E_1cb}$ उन्मूलन </div> <div style='float: right; width:30%; text-align: left;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/2185d3e4-d884-458f-2be6-544cb916e000/public" style='width:50%;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ <span style="color:blue">Elimination reaction</span> $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_1$ elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - $E_1$ is a model to explain a particular type of chemical elimination reaction. $E_1$ stands for unimolecular elimination and has the following specifications: 1. It is a two-step process of elimination: ionization and deprotonation. - Ionization: The carbon-halogen bond breaks to give a carbocation intermediate. - Deprotonation: Deprotonation of the carbocation gives the alkene. 2. $E_1$ reaction typically takes place with tertiary alkyl halides $\left(\mathrm{R} _3 \mathrm{CX}\right)$, but is possible with some secondary alkyl halides. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - $E_1$ एक विशेष प्रकार की रासायनिक उन्मूलन प्रतिक्रिया को समझाने वाला एक मॉडल है। $E_1$ का अर्थ है एक-आणविक उन्मूलन और इसमें निम्नलिखित विशिष्टताएँ हैं: 1. यह उन्मूलन की दो-चरणीय प्रक्रिया है: आयनीकरण और अवक्षेपण। - आयनीकरण: कार्बन-हैलोजन बंधन एक कार्बोकेशन मध्यवर्ती देने के लिए टूट जाता है। - अवक्षेपण: कार्बोधनायन के अवक्षेपण से एल्कीन प्राप्त होता है। 2. $E_1$ प्रतिक्रिया आम तौर पर तृतीयक एल्काइल हैलाइडों के साथ होती है $\left(\mathrm{R} _3 \mathrm{CX}\right)$, लेकिन कुछ द्वितीयक एल्काइल हैलाइडों के साथ संभव है। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ <span style="color:blue">$E_1$ elimination</span> $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_1$ elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> 3. The reaction rate is influenced only by the concentration of the alkyl halide because carbocation formation is the slowest step, known as the rate-determining step. Therefore, first-order kinetics apply (unimolecular). 4. The reaction usually occurs in the complete absence of a base or the presence of only a weak base (acidic conditions and high temperature). 5. The reaction gives thermodymaically stable product that is Saytzeff. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> 3. प्रतिक्रिया दर केवल एल्काइल हैलाइड की सांद्रता से प्रभावित होती है क्योंकि कार्बोकेशन गठन सबसे धीमा चरण है, जिसे दर-निर्धारण चरण के रूप में जाना जाता है। इसलिए, प्रथम-क्रम गतिकी लागू होती है (एक-आण्विक)। 4. प्रतिक्रिया आमतौर पर आधार की पूर्ण अनुपस्थिति या केवल कमजोर आधार (अम्लीय स्थिति और उच्च तापमान) की उपस्थिति में होती है। 5. प्रतिक्रिया से थर्मोडायमिक रूप से स्थिर उत्पाद मिलता है जो कि सैत्ज़ेफ़ है। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ <span style="color:blue">$E_1$ elimination</span> $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_1$ mechanism Example </B></Primary> <hr> <main> <div style='float: left; width:35%; text-align: left;font-size:23px'> - $E_1$ describes an elimination reaction (E) in which the ratedetermining step is unimolecular (1) and does not involve the base. - The leaving group leaves in this step, and the proton is removed in a separate second step. Tertiary-butyl bromide undergoes elimination reaction in presence of ethanol, a weak base to give isobutene </div> <div style='float: right; width:35%; text-align: left;font-size:23px'> - $E_1$ एक उन्मूलन प्रतिक्रिया (E) का वर्णन करता है जिसमें दर निर्धारण चरण एक-आण्विक (1) है और इसमें आधार शामिल नहीं है। - छोड़ने वाला समूह इस चरण में निकल जाता है, और प्रोटॉन एक अलग दूसरे चरण में हटा दिया जाता है। तृतीयक-ब्यूटाइल ब्रोमाइड इथेनॉल की उपस्थिति में उन्मूलन प्रतिक्रिया से गुजरता है, जो आइसोब्यूटीन देने के लिए एक कमजोर आधार है </div> <div style='float: right; width:30%; text-align: left;font-size:23px'> <br> <br> <br> <br> 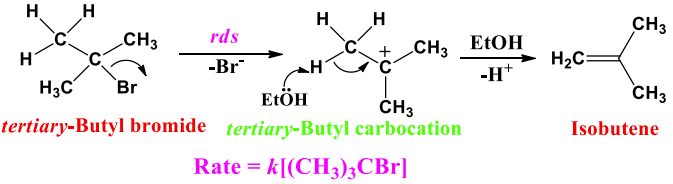 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ <span style="color:blue">$E_1$ mechanism Example</span> $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_2$ Elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - $E_2$ is a single step elimination, with a single transition state. - It is typically undergone by primary substituted alkyl halides, but is possible with some secondary alkyl halides and other compounds. - The reaction rate is second order, because it's influenced by both the alkyl halide and the base (bimolecular). - It requires antiperiplanar structure. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - $E_2$ एक एकल संक्रमण स्थिति के साथ एक एकल चरण उन्मूलन है। - यह आम तौर पर प्राथमिक प्रतिस्थापित एल्काइल हैलाइडों से गुजरता है, लेकिन कुछ माध्यमिक एल्काइल हैलाइडों और अन्य यौगिकों के साथ संभव है। - प्रतिक्रिया दर दूसरे क्रम की है, क्योंकि यह एल्काइल हैलाइड और बेस (द्विआणविक) दोनों से प्रभावित होती है। - इसके लिए एंटीपरिप्लानर संरचना की आवश्यकता होती है। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ <span style="color:blue">$E_2$ Elimination</span> $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_2$ Elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - An antiperiplanar transition state has staggered conformation with lower energy than a synperiplanar transition state which is in eclipsed conformation with higher energy. The reaction mechanism involving staggered conformation is more favorable for $E_2$ reactions (unlike $E_1$ reactions). - $E_2$ typically uses a strong base. It must be strong enough to remove a weakly acidic hydrogen. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - एक एंटीपरिप्लानर संक्रमण अवस्था में कम ऊर्जा के साथ कंपित संरचना होती है, जबकि एक सिन्परिप्लानर संक्रमण अवस्था में उच्च ऊर्जा के साथ ग्रहणीय संरचना होती है। कंपित संरचना से युक्त प्रतिक्रिया तंत्र $E_2$ प्रतिक्रियाओं के लिए अधिक अनुकूल है ($E_1$ प्रतिक्रियाओं के विपरीत)। - $E_2$ आमतौर पर एक मजबूत आधार का उपयोग करता है। यह कमजोर अम्लीय हाइड्रोजन को हटाने के लिए पर्याप्त मजबूत होना चाहिए। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ <span style="color:blue">$E_2$ Elimination</span> $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:35px ; text-align:center"><B> Example of $E_2$ elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - n-Propyl bromide undergoes elimination reaction in presence of ethanol, a strong base than ethanol itself, to give propene. Mechanism of $E_2$ reaction is shown in Figure: - It can give both Saytzeff and Hofmann elimination </div> <div style='float: right; width:35%; text-align: left;font-size:23px'> - एन-प्रोपाइल ब्रोमाइड प्रोपेन देने के लिए इथेनॉल की उपस्थिति में उन्मूलन प्रतिक्रिया से गुजरता है, जो इथेनॉल से भी अधिक मजबूत आधार है। $E_2$ प्रतिक्रिया का तंत्र चित्र में दिखाया गया है: - यह सैटज़ेफ़ और हॉफ़मैन दोनों को उन्मूलन दे सकता है </div> <div style='float: right; width:30%; text-align: left;font-size:23px'> 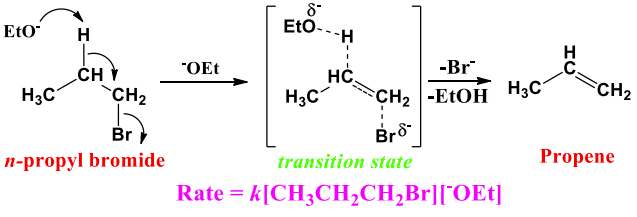 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ <span style="color:blue">Example of $E_2$ elimination</span> $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Saytzeff vs Hofmann </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - **Saytzeff** (working on RBr compounds) states that hydrogen will be eliminated preferentially from that β-carbon atom which is attached with least number of hydrogen atom/s. - Therefore, according Saytzeff rule ‘that alkene will predominate which has most alkyl substituents on the double bond carbons.’ </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - **सैट्ज़ेफ़** (आरबीआर यौगिकों पर काम करते हुए) का कहना है कि हाइड्रोजन को उस β-कार्बन परमाणु से प्राथमिकता से हटा दिया जाएगा जो कम से कम संख्या में हाइड्रोजन परमाणुओं से जुड़ा हुआ है। - इसलिए, सैत्ज़ेफ़ नियम के अनुसार 'वह एल्कीन प्रबल होगा जिसमें दोहरे बंधन कार्बन पर सबसे अधिक एल्काइल प्रतिस्थापन होंगे।' </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/1b06a4be-7987-41db-0ca7-1c0c153dc500/public" style='width:50;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ <span style="color:blue">Saytzeff vs Hofmann</span> $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Saytzeff vs Hofmann </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - **Hoffman** (working on RNMe3 + compounds) states that hydrogen will be eliminated preferentially from that β-carbon atom which is attached with most number of hydrogen atoms. - Therefore, according to Hofmann rule ‘that alkene will predominate which has least alkyl substituents on the double bond carbons.’ </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - **हॉफमैन** (RNMe3 + यौगिकों पर काम करते हुए) का कहना है कि हाइड्रोजन को उस β-कार्बन परमाणु से प्राथमिकता से हटा दिया जाएगा जो सबसे अधिक संख्या में हाइड्रोजन परमाणुओं से जुड़ा हुआ है। - इसलिए, हॉफमैन नियम के अनुसार 'वह एल्कीन प्रबल होगा जिसके दोहरे बंधन कार्बन पर कम से कम एल्काइल प्रतिस्थापन होंगे।' </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/b751ee1a-1aef-4d1a-136c-3d703af59d00/public" style='width:50;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ <span style="color:blue">Saytzeff vs Hofmann</span> $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_1$cb elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> - An elimination reaction that happens when a compound bearing a poor leaving group and an acidic hydrogen is treated with a base. - $E_1{cB}$ stands for Elimination Unimolecular conjugate Base. - The reaction is unimolecular from the conjugate base of the starting compound, which in turn is formed by deprotonation of the starting compound by a suitable base. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> - एक उन्मूलन प्रतिक्रिया जो तब होती है जब एक खराब छोड़ने वाले समूह और एक अम्लीय हाइड्रोजन वाले यौगिक को एक आधार के साथ इलाज किया जाता है। - $E_1{cB}$ का मतलब एलिमिनेशन यूनिमोलेक्यूलर कंजुगेट बेस है। - प्रतिक्रिया प्रारंभिक यौगिक के संयुग्म आधार से एक-आणविक होती है, जो बदले में एक उपयुक्त आधार द्वारा प्रारंभिक यौगिक के अवक्षेपण से बनती है। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ <span style="color:blue">$E_1$cb elimination</span> $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> $E_1$cb elimination </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> The electron withdrawing group (EWG) can be a carbonyl group (keto, aldehyde, ester), a nitro group, an electron deficient aromatic group etc. Dehydration of aldol is the most common $E_1{cB}$ reaction </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> इलेक्ट्रॉन निकालने वाला समूह (ईडब्ल्यूजी) एक कार्बोनिल समूह (कीटो, एल्डिहाइड, एस्टर), एक नाइट्रो समूह, एक इलेक्ट्रॉन की कमी वाला सुगंधित समूह आदि हो सकता है। एल्डोल का निर्जलीकरण सबसे आम है $E_1{cB} $प्रतिक्रिया </div> <div style='float: left; width:100%; text-align: center;font-size:23px'> 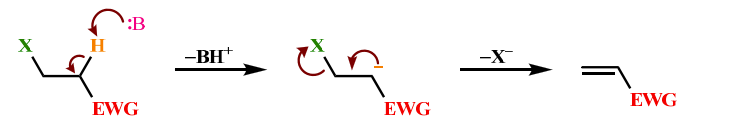 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ <span style="color:blue">$E_1$cb elimination</span> $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Substitution vs Elimination reaction </B></Primary> <hr> <main> <div style='float: left; width:99%; text-align: center;font-size:23px'> <img src="https://imagedelivery.net/YfdZ0yYuJi8R0IouXWrMsA/813fa561-6045-45bb-e29d-624e4f8ecb00/public" style='width:40%;'> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ <span style="color:blue">Substitution vs Elimination reactiuon</span> $\rarr$ Reaction with metals $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Reaction with metals </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:21px'> - Most organic chlorides, bromides and iodides react with certain metals to give compounds containing carbon-metal bonds. - Such compounds are known as organo-metallic compounds. - An important class of organo-metallic compounds discovered by Victor Grignard in 1900 is alkyl magnesium halide, RMgX, referred as Grignard Reagents. - These reagents are obtained by the reaction of haloalkanes with magnesium metal in dry ether. $$ \mathrm{CH} _3 \mathrm{CH} _2 \mathrm{Br}+\mathrm{Mg} \xrightarrow{\text { dry ether }} \underset{\text { Grignard reagent }}{\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{MgBr}} $$ </div> <div style='float: right; width:45%; text-align: left;font-size:21px'> - अधिकांश कार्बनिक क्लोराइड, ब्रोमाइड और आयोडाइड कुछ धातुओं के साथ प्रतिक्रिया करके कार्बन-धातु बंधन वाले यौगिक देते हैं। - ऐसे यौगिकों को ऑर्गेनो-मेटालिक यौगिक के रूप में जाना जाता है। - 1900 में विक्टर ग्रिग्नार्ड द्वारा खोजे गए ऑर्गेनो-मेटालिक यौगिकों का एक महत्वपूर्ण वर्ग एल्काइल मैग्नीशियम हैलाइड, आरएमजीएक्स है, जिसे ग्रिग्नार्ड अभिकर्मक कहा जाता है। - ये अभिकर्मक शुष्क ईथर में मैग्नीशियम धातु के साथ हैलोऐल्केन की अभिक्रिया से प्राप्त होते हैं। $$ \mathrm{CH} _3 \mathrm{CH} _2 \mathrm{Br}+\mathrm{Mg} \xrightarrow{\text { शुष्क ईथर }} \underset{\text { ग्रिग्नार्ड अभिकर्मक }}{\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{MgBr}} $$ </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$<span style="color:blue"> Reaction with metals</span> $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Reaction with metals </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> ##### Wurtz reaction Alkyl halides react with sodium in dry ether to give hydrocarbons containing double the number of carbon atoms present in the halide. This reaction is known as Wurtz reaction. $$ 2 \mathrm{RX}+2 \mathrm{Na} \longrightarrow \mathrm{RR}+2 \mathrm{NaX} $$ </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> ##### वर्ट्ज़ प्रतिकरिया एल्काइल हैलाइड शुष्क ईथर में सोडियम के साथ प्रतिक्रिया करके ऐसे हाइड्रोकार्बन बनाते हैं जिनमें हैलाइड में मौजूद कार्बन परमाणुओं की संख्या दोगुनी होती है। इस प्रतिक्रिया को वर्ट्ज़ प्रतिक्रिया के नाम से जाना जाता है। $$ 2 \mathrm{RX}+2 \mathrm{Na} \longrightarrow \mathrm{RR}+2 \mathrm{NaX} $$ </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ <span style="color:blue">Reaction with metals</span> $\rarr$ Example </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> **Question:** Haloalkanes react with KCN to form alkyl cyanides as main product while AgCN forms isocyanides as the chief product. Explain. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> **सवाल:** हैलोऐल्केन KCN के साथ क्रिया करके मुख्य उत्पाद के रूप में एल्काइल सायनाइड बनाते हैं जबकि AgCN मुख्य उत्पाद के रूप में आइसोसाइनाइड्स बनाता है। व्याख्या करना। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> **Answer:** KCN is predominantly ionic and provides cyanide ions in solution. Although both carbon and nitrogen atoms are in a position to donate electron pairs, the attack takes place mainly through carbon atom and not through nitrogen atom since C—C bond is more stable than C—N bond. However, AgCN is mainly covalent in nature and nitrogen is free to donate electron pair forming isocyanide as the main product. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> **उत्तर:** केसीएन मुख्य रूप से आयनिक है और घोल में साइनाइड आयन प्रदान करता है। हालाँकि कार्बन और नाइट्रोजन दोनों परमाणु दान करने की स्थिति में हैं इलेक्ट्रॉन जोड़े, हमला मुख्य रूप से कार्बन परमाणु और के माध्यम से होता है नाइट्रोजन परमाणु के माध्यम से नहीं क्योंकि C-C बंधन C-N की तुलना में अधिक स्थिर है गहरा संबंध। हालाँकि, AgCN प्रकृति में मुख्य रूप से सहसंयोजक है और नाइट्रोजन मुक्त है मुख्य उत्पाद के रूप में आइसोसायनाइड बनाने वाले इलेक्ट्रॉन युग्म का दान करना। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> **Question:** In the following pairs of halogen compounds, which would undergo $\mathrm{S} _{\mathrm{N}} 2$ reaction faster? </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> **सवाल:** हैलोजन यौगिकों के निम्नलिखित युग्मों में, कौन सा $\mathrm{S} _{\mathrm{N}} 2$ प्रतिक्रिया तेजी से करेगा? </div> <div style='float: left; width:100%; text-align: left;font-size:23px'> 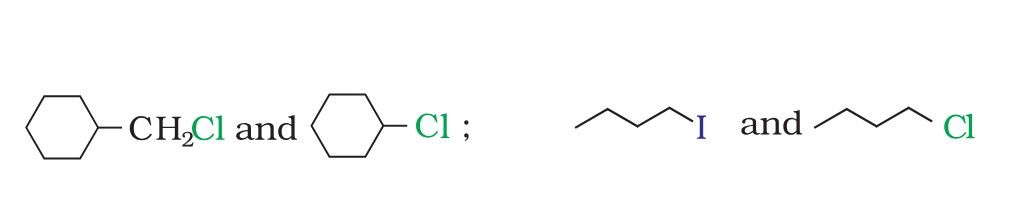 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:35%; text-align: left;font-size:21px'> **Answer:** It is primary halide and therefore undergoes $\mathrm{S} _{\mathrm{N}} 2$ reaction faster. As iodine is a better leaving group because of its large size, it will be released at a faster rate in the presence of incoming nucleophile. </div> <div style='float: right; width:35%; text-align: left;font-size:21px'> **उत्तर:** यह प्राथमिक हैलाइड है और इसलिए $\mathrm{S} _{\mathrm{N}} 2$ तेजी से प्रतिक्रिया करता है। चूंकि आयोडीन अपने बड़े आकार के कारण बेहतर छोड़ने वाला समूह है, इसलिए यह आने वाले न्यूक्लियोफाइल की उपस्थिति में तेज दर से जारी किया जाएगा। </div> <div style='float: left; width:25%; text-align: left;font-size:23px'> 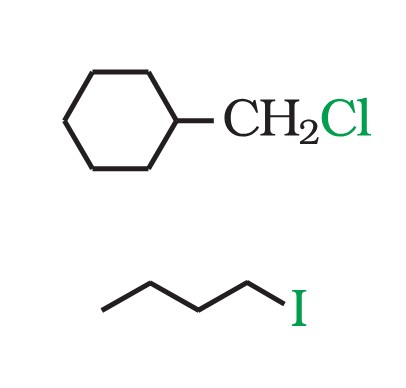 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> Question: Predict the order of reactivity of the following compounds in $\mathrm{S} _{\mathrm{N}} 1$ and $\mathrm{S} _{\mathrm{N}} 2$ reactions: (i) The four isomeric bromobutanes <p> (ii) $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm{Br},$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br},$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}, $ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C} _2\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$ </p> </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> प्रश्न: $\mathrm{S} _{\mathrm{N}} 1$ और $\mathrm{S} _{\mathrm{N}} 2$ प्रतिक्रियाओं में निम्नलिखित यौगिकों की प्रतिक्रियाशीलता के क्रम की भविष्यवाणी करें: (i) चार आइसोमेरिक ब्रोमोब्यूटेन <p> (ii) $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm{Br},$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br},$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}, $ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C} _2\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$ </p> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> **Solution** (i) <p> $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}<\left(\mathrm{CH} _3\right)_2 $ $\mathrm{CHCH} _2 \mathrm{Br}<\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br})$ $\mathrm{CH} _3<\left(\mathrm{CH} _3\right)_3 \mathrm{CBr}\left(\mathrm{S} _{\mathrm{N}} 1\right) $ $ \mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}>\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2$ $\mathrm{Br}>\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH} _3>\left(\mathrm{CH} _3\right)_3 \mathrm{CBr}\left(\mathrm{S} _{\mathrm{N}} 2\right)$ </p> </div> <div style='float: right; width:45%; text-align: left;font-size:21px'> **समाधान** (i) <p> $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}<\left(\mathrm{CH} _3\right)_2 $ $\mathrm{CHCH} _2 \mathrm{Br}<\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br})$ $\mathrm{CH} _3<\left(\mathrm{CH} _3\right)_3 \mathrm{CBr}\left(\mathrm{S} _{\mathrm{N}} 1\right) $ $ \mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}>\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2$ $\mathrm{Br}>\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH} _3>\left(\mathrm{CH} _3\right)_3 \mathrm{CBr}\left(\mathrm{S} _{\mathrm{N}} 2\right)$ </p> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> <p> Of the two primary bromides, the carbocation intermediate derived from $\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2 \mathrm{Br}$ is more stable than derived from $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}$ because of greater electron donating inductive effect of $\left(\mathrm{CH} _3\right)_2 \mathrm{CH}$ - group. Therefore, $\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2 \mathrm{Br}$ is more reactive than $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}$ in $\mathrm{S} _{\mathrm{N}} 1$ reactions. $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH} _3$ is a secondary bromide and $\left(\mathrm{CH} _3\right)_3 \mathrm{CBr}$ is a tertiary bromide. Hence the above order is followed in $\mathrm{S} _{\mathrm{N}} 1$. The reactivity in $\mathrm{S} _{\mathrm{N}} 2$ reactions follows the reverse order as the steric hinderance around the electrophilic carbon increases in that order. </p> </div> <div style='float: right; width:45%; text-align: left;font-size:20px'> <p> दो प्राथमिक ब्रोमाइडों में से, $\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2 \mathrm{Br}$ से प्राप्त कार्बोकेशन मध्यवर्ती, $\mathrm{CH} _3 से प्राप्त कार्बोकेशन मध्यवर्ती से अधिक स्थिर है \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{CH} _2 \mathrm{Br}$ अधिक इलेक्ट्रॉन दान के कारण $\left(\mathrm{CH} _3\right)_2 \mathrm{CH }$ - समूह. इसलिए, $\left(\mathrm{CH} _3\right)_2 \mathrm{CHCH} _2 \mathrm{Br}$ $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH} से अधिक प्रतिक्रियाशील है _2 \mathrm{CH} _2 \mathrm{Br}$ $\mathrm{S} _{\mathrm{N}} 1$ प्रतिक्रियाओं में। $\mathrm{CH} _3 \mathrm{CH} _2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH} _3$ एक द्वितीयक ब्रोमाइड है और $\left(\mathrm{CH} _3\right) _3 \mathrm{CBr}$ एक तृतीयक ब्रोमाइड है। इसलिए $\mathrm{S} _{\mathrm{N}} 1$ में उपरोक्त क्रम का पालन किया जाता है। $\mathrm{S} _{\mathrm{N}} 2$ प्रतिक्रियाओं में प्रतिक्रियाशीलता विपरीत क्रम का पालन करती है क्योंकि इलेक्ट्रोफिलिक कार्बन के चारों ओर स्थैतिक बाधा उस क्रम में बढ़ती है। </p> </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> (ii) $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C}\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm{Br}\left(\mathrm{S} _{\mathrm{N}} 1\right)$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C}\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm{Br}\left(\mathrm{S} _{\mathrm{N}} 2\right)$ Of the two secondary bromides, the carbocation intermediate obtained from $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$ is more stable than obtained from $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}$ because it is stabilised by two phenyl groups due to resonance. </div> <div style='float: right; width:45%; text-align: left;font-size:21px'> (ii) $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C}\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm {Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}>\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm {Br}\left(\mathrm{S} _{\mathrm{N}} 1\right)$ $\mathrm{C} _6 \mathrm{H} _5 \mathrm{C}\left(\mathrm{CH} _3\right)\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm {C} _6 \mathrm{H} _5\right) \mathrm{Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm {Br}<\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH} _2 \mathrm{Br}\left(\mathrm{S} _{\mathrm{N}} 2\right)$ में से दो द्वितीयक ब्रोमाइड, $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$ से प्राप्त कार्बोकेशन मध्यवर्ती $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right)\mathrm{Br}$ से प्राप्त की तुलना में $ अधिक स्थिर है क्योंकि यह दो फिनाइल द्वारा स्थिर होता है अनुनाद के कारण समूह। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> Therefore, the former bromide is more reactive than the latter in $\mathrm{S} _{\mathrm{N}} 1$ reactions. A phenyl group is bulkier than a methyl group. Therefore, $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$ is less reactive than $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}$ in $\mathrm{S} _{\mathrm{N}} 2$ reactions. </div> <div style='float: right; width:45%; text-align: left;font-size:23px'> इसलिए, $\mathrm{S} _{\mathrm{N}} 1$ प्रतिक्रियाओं में पहला ब्रोमाइड बाद वाले की तुलना में अधिक प्रतिक्रियाशील है। फिनाइल समूह मिथाइल समूह की तुलना में भारी होता है। इसलिए, $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{C} _6 \mathrm{H} _5\right) \mathrm{Br}$, से कम प्रतिक्रियाशील है $\mathrm{C} _6 \mathrm{H} _5 \mathrm{CH}\left(\mathrm{CH} _3\right) \mathrm{Br}$ in $\mathrm{S} _{\mathrm{N}} 2 $प्रतिक्रियाएँ। </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:49%; text-align: left;font-size:23px'> **Question: ** Identify chiral and achiral molecules in each of the following pair of compounds. (Wedge and Dash representations according to Class XI. </div> <div style='float: right; width:45%; text-align: left;font-size:21px'> **सवाल: ** निम्नलिखित जोड़ी में से प्रत्येक में काइरल और अचिरल अणुओं की पहचान करें यौगिक. (कक्षा XI के अनुसार वेज और डैश प्रतिनिधित्व। <div style='float: left; width:99%; text-align: center;font-size:21px'> 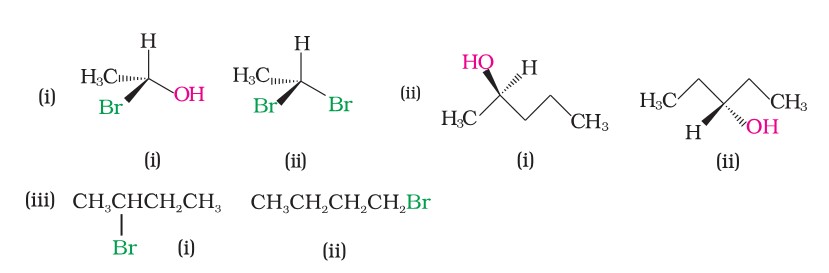 </div> </main> <hr> <footer style="font-size:18px"> Elimination reactions $\rarr$ $S_N i$ reaction $\rarr$ Elimination reaction $\rarr$ $E_1$ elimination $\rarr$ $E_1$ mechanism Example $\rarr$ $E_2$ Elimination $\rarr$ Example of $E_2$ elimination $\rarr$ Saytzeff vs Hofmann $\rarr$ $E_1$cb elimination $\rarr$ Substitution vs Elimination reactiuon $\rarr$ Reaction with metals $\rarr$ <span style="color:blue">Example</span> </footer>
<Success style=" font-size:25px ; text-align:center"><B>Haloalkane and Haloarene</B></Success> <Primary style=" font-size:23px ; text-align:center"><B> Example </B></Primary> <hr> <main> <div style='float: left; width:99%; text-align: left;font-size:23px'> **Solution:** 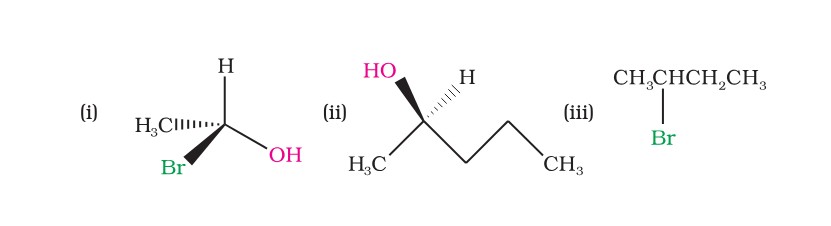 </div> </div> </div> <script src="/reveal/dist/reveal.js"></script> <script src="/reveal/plugin/markdown/markdown.js"></script> <script src="/reveal/plugin/highlight/highlight.js"></script> <script src="/reveal/plugin/math/math.js"></script> <script src="/reveal/plugin/anything/plugin.js"></script> <script src="/reveal/plugin/notes/notes.js"></script> <script src="/reveal/plugin/chart/Chart.min.js"></script> <script src="/reveal/plugin/chart/plugin.js"></script> <script src="/reveal/plugin/menu/menu.js"></script> <script src="/reveal/plugin/highlight/highlight.js"></script> <script src="/reveal/plugin/audio-slideshow/plugin.js"></script> <script src="/reveal/plugin/audio-slideshow/recorder.js"></script> <script src="/reveal/plugin/audio-slideshow/RecordRTC.js"></script> <script src="/reveal/plugin/copycode/copycode.js"></script> <script src="/reveal/plugin/RevealEditor-master/revealeditor.js"></script> <script src="/reveal/plugin/jump/jump.js"></script> <script src="/reveal/plugin/zoom/zoom.js"></script> <script src="https://cdnjs.cloudflare.com/ajax/libs/clipboard.js/2.0.6/clipboard.min.js"></script> <script> Reveal.initialize({ slideNumber: true, controls: true, controlsTutorial: true, progress: true, transition: 'fade', highlight: { escapeHTML: false }, customcontrols: { controls: [ { icon: '<i class="fa fa-pen-square"></i>', title: 'Toggle chalkboard (B)', action: 'RevealChalkboard.toggleChalkboard();' }, { icon: '<i class="fa fa-pen"></i>', title: 'Toggle notes canvas (C)', action: 'RevealChalkboard.toggleNotesCanvas();' } ] }, plugins: [RevealMath.KaTeX,RevealMarkdown, RevealHighlight, RevealNotes, RevealAnything, RevealMenu, RevealChalkboard, RevealChart, RevealAudioSlideshow, RevealAudioRecorder, CopyCode, RevealZoom], }); function transformCallouts() { var slides = document.querySelectorAll('.reveal .slides section'); slides.forEach(function (slide) { var data = document.getElementsByTagName("Success"); for (let i = 0; i < data.length; i++) { data[i].classList.add("callout"); data[i].classList.add("callout-success"); } var data = document.getElementsByTagName("Default"); for (let i = 0; i < data.length; i++) { data[i].classList.add("callout"); data[i].classList.add("callout-default"); } var data = document.getElementsByTagName("Warning"); for (let i = 0; i < data.length; i++) { data[i].classList.add("callout"); data[i].classList.add("callout-warning"); } var data = document.getElementsByTagName("Primary"); for (let i = 0; i < data.length; i++) { data[i].classList.add("callout"); data[i].classList.add("callout-primary"); } var data = document.getElementsByTagName("Danger"); for (let i = 0; i < data.length; i++) { data[i].classList.add("callout"); data[i].classList.add("callout-danger"); } }); }; function addrfit() { var slides = document.querySelectorAll('.reveal'); slides.forEach(function (slide) { var temp = document.getElementsByTagName("h2"); if (temp.length > 0) { for (let i = 0; i < temp.length; i++) { temp[i].classList.add("r-fit-text"); } } var temp3 = document.getElementsByTagName("h1"); if (temp3.length > 0) { for (let i = 0; i < temp3.length; i++) { temp3[i].classList.add("r-fit-text"); } } var temp6 = document.getElementsByClassName("text-container"); if (temp6.length > 0) { for (let i = 0; i < temp6.length; i++) { var charcount = 0; var ptags = temp6[i].getElementsByTagName("p"); try { for (let j = 0; j < ptags.length; j++) { temp = ptags[j].outerText.replaceAll(" ", ""); temp = temp.replaceAll("\n", ""); charcount += temp.length; } } catch (err) { console.log(err); } var font = 35; if (charcount > 50 && charcount < 100) { font = 35; } else if (charcount > 100 && charcount < 120) { font = 33; } else if (charcount > 120 && charcount < 150) { font = 33; } else if (charcount > 150 && charcount < 170) { font = 31; } else if (charcount > 170 && charcount < 200) { font = 30; } else if (charcount > 200 && charcount < 230) { font = 29; } else if (charcount > 230 && charcount < 250) { font = 28; } else if (charcount > 250 && charcount < 270) { font = 27; } else if (charcount > 270 && charcount < 300) { font = 25; } else if (charcount > 300 && charcount < 330) { font = 23; } else if (charcount > 330 && charcount < 360) { font = 24; } else if (charcount > 360 && charcount < 390) { font = 22; } else if (charcount > 390 && charcount < 420) { font = 21; } else if (charcount > 420) { font = 20; } temp6[i].style.fontSize = `${font}px`; } } }) } Reveal.addEventListener('ready', addrfit); Reveal.addEventListener('ready', transformCallouts); </script> <script> function adjustFontSize(element) { let fontSize = parseInt(window.getComputedStyle(element).fontSize); const parentWidth = element.parentNode.offsetWidth; while (element.scrollHeight > element.offsetHeight || element.scrollWidth > parentWidth) { fontSize -= 1; element.style.fontSize = fontSize + 'px'; } } function checkOverflow() { const elements = document.querySelectorAll('.left, .right'); elements.forEach(element => { adjustFontSize(element); }); } window.addEventListener('load', checkOverflow); window.addEventListener('resize', checkOverflow); </script> </body> </html>